
 Juste après la Seconde Guerre mondiale, un monde plein d’espoir a produit une nouvelle génération formidable.
Juste après la Seconde Guerre mondiale, un monde plein d’espoir a produit une nouvelle génération formidable.
La plupart d’entre eux ont bien réussi. Ils ont travaillé toute leur vie et sont prêts à payer pour des aides pharmaceutiques qui prolongeront et faciliteront leur « âge d’or ».
Ils veulent vieillir, mais ils veulent vieillir avec grâce, en gardant leurs compétences de jeunesse. Ils ne veulent pas passer leurs dernières années dans un fauteuil roulant ou dans un lit de soin avec un pot.
Ils veulent rester mobiles et avoir une vie sexuelle saine. Le succès du Viagra de Phizers en est la preuve.
Les autorités du monde entier sont confrontées à des coûts de santé énormes en raison du vieillissement du baby-boom.
La perte constante de masse osseuse (ostéoporose) et de masse musculaire maigre (sarcopénie) qui accompagne le vieillissement met de plus en plus à contribution nos systèmes de santé.
Elle touche des millions de personnes âgées dans le monde.
La perte de masse, de force et de fragilité musculaires liée à l’âge, causée par la diminution des niveaux d’hormones essentielles dans le corps, telles que les hormones sexuelles et l’hormone de croissance, les empêche d’accomplir les tâches quotidiennes et augmente le risque de chutes et de démangeaisons osseuses dues à l’ostéoporose.
Il s’agit non seulement d’un problème socio-économique majeur, mais aussi d’un problème médical et financier, et il est important pour améliorer le bien-être général de toutes ces personnes âgées.
Tout cela a conduit à une augmentation des financements et à la nécessité d’une recherche scientifique sur la prévention des maladies liées à l’âge.
Nous savions déjà que l’administration exogène de rhGH et d’hormones sexuelles telles que la testostérone (HRT) pouvait améliorer le bien-être général des personnes âgées.
La testostérone elle-même est naturelle et n’est donc pas brevetable. Pour la plupart des analogues de la testostérone, le brevet a expiré depuis longtemps.
Mais le HRT/TRT et la lutte contre le vieillissement deviennent un énorme potentiel de rentabilité.
Au cours des dernières décennies, le gouvernement, les sociétés de suppléments, les grandes sociétés pharmaceutiques et la communauté médicale ont diabolisé les stéroïdes en les présentant comme un médicament malin ayant d’horribles effets secondaires, car ils vendaient plutôt des médicaments brevetés.
En raison de toutes ces histoires d’horreur et de la stigmatisation liée au fait d’être des médicaments améliorant les performances (DAP), alias le dopage, les stéroïdes androgènes anabolisants ne peuvent pas être mis sur le marché comme « sauveurs de vie ».
C’est pourquoi nous avons mis au point une nouvelle structure qui s’éloigne de la structure à quatre anneaux de carbone et un nouveau nom fantaisiste
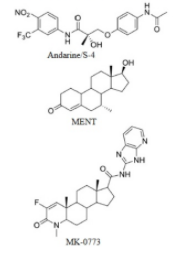 Structurellement, le SARM peut être classé en SARM stéroïdien et non stéroïdien. Le SARM stéroïdien est formé en modifiant la structure chimique de la molécule de testostérone.
Structurellement, le SARM peut être classé en SARM stéroïdien et non stéroïdien. Le SARM stéroïdien est formé en modifiant la structure chimique de la molécule de testostérone.
Comme MENT, qui n’a pas maintenu efficacement la suppression des spermatozoïdes nécessaire à la contraception hormonale masculine, des modèles animaux récents suggèrent que le SARM non stéroïdien pourrait être prometteur.
Les SARM non stéroïdiens sont des ligands qui activent le récepteur des androgènes tout comme les stéroïdes, mais il leur manque la structure de quatre anneaux de carbone fusionnés.
Techniquement parlant, les stéroïdes eux-mêmes sont sélectifs pour le récepteur des androgènes.
Et comme vous le verrez plus tard, il n’existe qu’un seul récepteur pour la testostérone et tous les autres stéroïdes anabolisants androgènes. et le SARM!
Pour le développement musculaire, l’objectif est de maximiser les effets anaboliques des composés stimulant la croissance tout en réduisant leurs effets androgènes.
Le terme « anabolique » fait référence aux propriétés de construction tissulaire du composé, notamment l’augmentation de la masse musculaire (rétention d’azote) et la diminution de la graisse corporelle.
Le terme « androgène » fait référence au développement accru des caractéristiques sexuelles masculines par le composé, y compris les changements de comportement et le développement du système de reproduction.
Les dérivés de stéroïdes ont été synthétisés avec des activités androgènes et anaboliques spécifiques qui sont déterminées par un essai biologique sur des rats castrés.
Les effets du composé sur l’activité myotropique du muscle releveur d’ani est utilisé comme mesure de l’activité anabolique.
La relation entre l’activité anabolique et androgène est la valeur Q ou l’indice anabolique du composé, une valeur supérieure à un indique que le composé est principalement de nature anabolique.
Ces valeurs Q peuvent varier entre les différents laboratoires en raison des méthodes non normalisées utilisées pour leur détermination.
Le muscle releveur ani peut également être androgène-dépendant, de sorte que les véritables mesures de l’activité anabolique devraient être basées sur des études de rétention d’azote dans tout le corps.
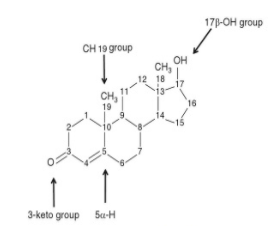
Les caractéristiques structurelles des stéroïdes qui sont liées à l’activité anabolique par rapport à l’activité androgène sont présentées dans le graphique de gauche.
Des études sur l’activité structurelle ont montré que la présence du groupe 3-céto, 5α-hydrogène et 17β-hydroxyle augmente l’affinité du stéroïde pour la liaison au récepteur des androgènes et les effets androgènes des stéroïdes.
L’élimination de la C19 (pour former des 19-non stéroïdes) augmente l’activité anabolique et réduit l’activité androgénique. L’oxydation de 17β-hydroxyl réduit l’activité androgène et la strification de ce groupe hydroxyle favorise l’activité anabolique.
La modification du cycle A par liaison au cycle pyrazole ou à l’atome d’oxygène en C2 entraîne une augmentation considérable de l’activité anabolique.
L’activité anabolique peut également être augmentée par alkylation dans la position 17α- ou 7α-.
En raison de la faible biovalidité orale, de l’hépatotoxicité possible et, en particulier, du manque de sélectivité tissulaire de certains stéroïdes, un grand nombre de composés androgènes non stéroïdiens, connus sous le nom de modulateurs sélectifs des récepteurs androgènes (SARM), ont été développés.
Les premiers de ces composés développés étaient des antagonistes des androgènes, mais des agonistes ont également été produits.
Les recherches en cours conduiront au développement du SARM avec des préférences sélectives pour les tissus ou les activités individuelles.
Les androgènes augmentent la rétention des protéines du corps, ce qui peut être le résultat d’une augmentation de la synthèse des protéines ou d’une diminution de leur dégradation.
Alors que la testostérone augmente la synthèse des protéines, la trenbolone favorise la croissance musculaire en ralentissant la dégradation des protéines.
Comme le nombre de fibres musculaires dont une personne dispose est fixé à la naissance ou peu après, la croissance musculaire ultérieure se fait par hypertrophie plutôt que par hyperplasie.
Cela nécessite une augmentation du nombre de myonucléus, qui proviennent de cellules satellites qui fusionnent avec le muscle fie.
Le traitement aux androgènes entraîne une augmentation du nombre de cellules satellites en fonction de la dose.
Les stéroïdes anabolisants peuvent agir par un mécanisme direct par interaction ou par des méthodes indirectes.
Les mécanismes indirects comprennent l’aromatisation à l’œstrogène et l’action par le biais du récepteur d’œstrogène ou la modulation de la production d’autres hormones, telles que l’hormone de croissance, l’hormone thyroïdienne et l’insuline.
Les effets directs des androgènes sont médiés par l’interaction avec le récepteur des androgènes.
Un grand nombre de composés androgènes différents ont été développés, connus sous le nom de modulateurs sélectifs des récepteurs androgéniques (SARM).
Cependant, un seul récepteur d’androgène a été identifié et cloné.
Le gène AR est situé sur le chromosome X et code une protéine de 918 acides aminés.
En tant que membre de la famille des récepteurs de facteurs de transcription nucléaire, il contient des domaines protéiques qui peuvent activer ou supprimer l’activité.
Ces domaines sont exposés en se liant à des hormones pour permettre des interactions avec divers co-activateurs ou co-répresseurs.
Les effets différentiels des androgènes dans les divers tissus peuvent être dus à des différences dans les niveaux de cofacteurs affectant la PR, ou à la présence de protéines uniques qui interagissent avec la PR comme ARIP-3, qui est spécifique aux testicules.
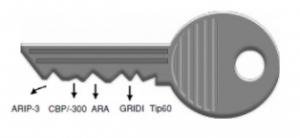
En outre, la liaison d’un SARM donné à la RA peut provoquer un changement de conformation unique qui expose des domaines particuliers permettant l’interaction de cofacteurs spécifiques.
Cela conduirait à la régulation sélective de gènes individuels dans des tissus spécifiques par la RA.
Les recherches en cours conduiront au développement du SARM avec des préférences sélectives pour des tissus ou des activités individuels.
 La testostérone peut être irréversiblement réduite par l’enzyme 5α-reductase dans certains tissus pour former la 5α-dihydrotestostérone, qui peut être métabolisée en 17 stéroïdes cétoïdes et en métabolites polaires qui auront des caractéristiques différentes de liaison à l’AR.
La testostérone peut être irréversiblement réduite par l’enzyme 5α-reductase dans certains tissus pour former la 5α-dihydrotestostérone, qui peut être métabolisée en 17 stéroïdes cétoïdes et en métabolites polaires qui auront des caractéristiques différentes de liaison à l’AR.
L’aromatisation des androgènes avec un groupe d’œstrogènes Δ-4-3-keto peut également être importante dans certains tissus car des effets similaires aux œstrogènes se produiront.
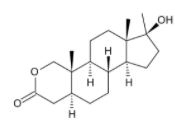
La réaction de l’aromatase peut être bloquée en supprimant la fonction du méthyle C19 (comme dans la nandrolone) ou en modifiant le cycle A (comme dans l’oxandrolone (à gauche) et le stanazol).
Les androgènes ont un effet primaire sur les muscles squelettiques en se liant à des récepteurs spécifiques dans le muscle.
Comme l’activité de l’enzyme 5α-reductase est faible dans les muscles squelettiques, la testostérone est la principale hormone pour l’action des androgènes dans les muscles.
Un nombre accru de récepteurs d’androgènes est trouvé lors de l’hypertrophie musculaire observée avec l’augmentation de l’exercice ou le traitement à l’oxandrolone, qui est un analogue synthétique de la testostérone qui ne peut pas être parfumé aux oestrogènes.
Le nombre de récepteurs androgènes libres est plus élevé chez les femelles et les castrats que chez les mâles intacts.
Un récepteur d’œstrogène a également été identifié, et la forme libre de ce récepteur est présente en plus grande quantité chez les hommes que chez les femmes.
Les stéroïdes se lient aux récepteurs dans le cytoplasme, et le complexe de récepteurs hormonaux entre dans le noyau pour stimuler la transcription de gènes hormonaux spécifiques.
Cela augmente la synthèse des protéines myophylles et sarcoplasmiques pour augmenter la masse musculaire globale.
Les androgènes peuvent fonctionner indirectement en augmentant la production de GH ou d’IGF-I, et une exposition antérieure aux androgènes peut préparer les cellules aux actions secondaires de l’IGF-I.
Les glucocorticoïdes peuvent augmenter la production de protéines de liaison à l’IGF pour diminuer la bioactivité de l’IGF.
Les stéroïdes anabolisants réduisent également la production de LH et de testostérone, retardent la maturation sexuelle et réduisent la croissance testiculaire et la spermatogenèse chez l’homme.
Il semble y avoir une relation réciproque entre la testostérone (une hormone anabolique) et le cortisol (une hormone catabolique) chez les hommes.
Les stéroïdes anabolisants peuvent potentiellement agir comme un antagoniste de l’action catabolique des glucocorticoïdes, en diminuant la concentration des glucocorticoïdes ou en déplaçant les glucocorticoïdes de leurs récepteurs.
Des études in vitro ont montré que la testostérone a une grande affinité avec le récepteur des glucocorticoïdes et peut donc empêcher l’action catabolique normale des protéines des glucocorticoïdes.
Il existe des preuves que les agents anabolisants ayant une activité œstrogénique augmentent les niveaux d’insuline dans le sang pour favoriser la croissance. Les oestrogènes augmentent le taux de croissance et l’efficacité alimentaire.
L’insuline a un effet anabolique sur le tissu adipeux et les muscles squelettiques, tandis que l’hormone thyroïdienne (T3) a un effet catabolique sur le tissu adipeux et une influence anabolique sur les muscles squelettiques.
Le terme « anabolique » désigne les composés qui augmentent la rétention d’azote. Plusieurs types de composés différents, tels que l’insuline, l’hormone de croissance, les β-agonistes et les stéroïdes, exercent des effets anabolisants.
Sélectivité tissulaire du stéroïde anabolisant 19-nor-4-androstènediol-3 bêta, 17 bêta-diol chez des rats Sprague Dawley mâles: stimulation sélective de la masse musculaire et de la densité minérale osseuse par rapport à la masse de la prostate.
Page et all 2008 : « La stimulation de la croissance de la prostate est une préoccupation majeure de la thérapie à la testostérone chez les hommes hypogonadiques âgés.
C’est pourquoi des modulateurs sélectifs des récepteurs androgènes non stéroïdiens à activité anabolique mais moins stimulants pour la prostate sont en cours de développement.
Les stéroïdes anabolisants peuvent présenter une sélectivité tissulaire similaire. Nous avons émis l’hypothèse que le stéroïde anabolisant 19-nor-4-androstènediol-3 bêta,17 bêta-diol (3 bêta,19-NA) augmenterait la masse musculaire, la masse maigre (LBM) et la densité minérale osseuse (BMD) avec une faible stimulation de la croissance de la prostate.
En résumé, le 3-bêta,19-NA augmente la masse musculaire et osseuse sans stimulation significative de la croissance de la prostate, ce qui suggère qu’il pourrait avoir certaines propriétés d’un modulateur sélectif des récepteurs androgènes des stéroïdes.
Les stéroïdes anabolisants tels que le 3beta19-NA devraient être étudiés plus avant afin de déterminer leurs mécanismes de sélectivité tissulaire et leurs effets chez l’homme ».
Sélectivité tissulaire et applications cliniques possibles de la trenbolone (17bêta-hydroxyestra-4,9,11-triène-3-one): puissant stéroïde anabolisant à activité androgénique et œstrogénique réduite. Yarrow et all 2010:
« Le développement de modulateurs sélectifs des récepteurs androgènes (SARM) a récemment été suggéré comme moyen de lutter contre les effets cataboliques néfastes de l’hypogonadisme, en particulier sur les muscles et les os du squelette, sans induire les effets androgènes indésirables (par exemple l’hypertrophie de la prostate et la polycythémie) associés à l’administration de testostérone.
La 17bêta-Hydroxyestra-4,9,11-triène-3-one (trenbolone ; 17bêta-TBOH), un analogue synthétique de la testostérone, pourrait être capable d’induire des effets similaires à ceux du SARM en se liant aux récepteurs androgènes (RA) avec une affinité environ trois fois supérieure à celle de la testostérone.
Il a été démontré qu’elle augmente la masse musculaire squelettique et la croissance osseuse et réduit l’adiposité chez diverses espèces de mammifères.
En plus de ses actions directes par le biais de l’AR, le 17 bêta-TBOH peut également exercer des effets anabolisants en modifiant l’action des facteurs de croissance endogènes ou en inhibant l’action des glucocorticoïdes.
Par rapport à la testostérone, la 17bêta-TBOH semble induire une croissance moindre dans les organes sensibles aux androgènes qui expriment largement l’enzyme 5alpha réductase (par exemple le tissu prostatique et les organes sexuels accessoires).
Les effets androgènes réduits sont dus au fait que le 17 bêta-TBOH est métabolisé en androgènes moins puissants in vivo; tandis que la testostérone subit une biotransformation spécifique aux tissus en stéroïdes plus puissants, la dihydrotestostérone et le 17 bêta-oestradiol, via les enzymes 5-alpha-réductase et aromatase, respectivement.
Ainsi, le métabolisme de la 17bêta-TBOH fournit une base pour de futures recherches visant à évaluer sa sécurité et son efficacité en tant que moyen de combattre les conditions de dépérissement musculaire et osseux, l’obésité et/ou les syndromes d’insensibilité aux androgènes chez l’homme, comme d’autres SARM actuellement en cours de développement ».
Remarque: l’étude ne porte pas sur « notre » trenbolone, mais sur un isomère 17-beta du trenbolone.